Il existe de nombreux types de contraception, les plus populaires aujourd’hui étant les méthodes barrières et hormonales.
L'un des types de médicaments contraceptifs hormonaux modernes est l'anneau contraceptif vaginal NovaRing.
Qu'est-ce que l'anneau vaginal NuvaRing ?
NuvaRing est un contraceptif hormonal combiné qui contient des microdoses d'œstrogènes (éthinylestradiol) et de progestatif (étonogestrel).
Le contraceptif est un petit anneau flexible (diamètre seulement 55 mm, épaisseur 8,5 mm), réalisé en matériau hypoallergénique. Après insertion dans le vagin, des microdoses d'hormones sont libérées quotidiennement depuis l'anneau (ce mécanisme d'action est obtenu grâce au système complexe de membranes qui le compose).
L'effet contraceptif, comme d'autres médicaments hormonaux, s'effectue en supprimant l'ovulation. De plus, les hormones augmentent la densité du mucus dans le col de l’utérus, empêchant ainsi la progression des spermatozoïdes.
Le principal avantage de l'anneau vaginal hormonal NuvaRing est l'absence de passage primaire dans le tractus gastro-intestinal et le foie, l'entrée d'hormones dans l'organisme en microdoses, ce qui réduit considérablement le risque d'effets secondaires liés à son utilisation par rapport à d'autres médicaments hormonaux.
Dans le même temps, l’efficacité contraceptive de l’anneau vaginal est élevée. L'indice de Pearl (un indicateur reflétant le nombre de femmes sur cent tombées enceintes en prenant le médicament au cours de l'année) lors de l'utilisation d'un anneau contraceptif est de 0,96. À titre de comparaison, lors de la prise de cotraceptifs oraux combinés, l'indice de Pearl est de 0,1 à 0,9.
En plus de son effet contraceptif, le médicament a également un effet positif sur le cycle menstruel, le rendant plus régulier et les menstruations moins douloureuses et moins abondantes.
Il est important de rappeler que l’anneau contraceptif ne protège pas contre les maladies sexuellement transmissibles ! Par conséquent, cette méthode de contraception convient aux femmes qui ont un partenaire sexuel permanent, ainsi qu'à l'absence d'infections sexuellement transmissibles chez les deux partenaires.
Contre-indications
Comme tout médicament hormonal, NuvaRing possède une liste assez longue de contre-indications.
Il existe également un certain nombre de maladies dans lesquelles l'utilisation d'un anneau vaginal est possible avec prudence (obésité, malformations cardiaques, etc.).
Une liste complète des contre-indications peut être trouvée dans les instructions du médicament. Par conséquent, si une femme souffre de l'une de ces maladies ou d'une prédisposition à celles-ci (y compris les maladies chez des proches), alors avant d'utiliser le médicament, vous devez évaluer les risques et les avantages possibles de son utilisation et éventuellement refuser de l'utiliser en faveur d'une autre méthode. de contraception.
Utilisation pendant la grossesse et l'allaitement
Si une femme souhaite tomber enceinte, elle doit arrêter de prendre le médicament et attendre le retour de son cycle naturel. En règle générale, une grossesse après l'arrêt de NuvaRing est possible dans un délai de 1 à 2 mois.
L'utilisation d'un anneau contraceptif pour les femmes pendant l'allaitement n'est pas non plus souhaitable. La composition du médicament peut affecter la lactation, en réduire la quantité et également modifier la composition du lait maternel.
Lorsqu'une femme est enceinte, l'anneau doit être retiré car il est contre-indiqué pendant la grossesse.
Mode d'emploi
L’anneau contraceptif NuvaRing est très pratique à utiliser car il ne nécessite pas de surveillance quotidienne. Après insertion, l'anneau reste dans le vagin pendant exactement 3 semaines, puis il doit être retiré le jour même de son insertion.
Après avoir retiré l'anneau, une pause de sept jours est prise, après quoi une nouvelle est introduite. Essentiellement, le principe est le même que lors de la prise de contraceptifs oraux combinés, sauf que dans ce cas, l'apport quotidien d'hormones dans le corps se fait indépendamment sans la participation de la femme.
Lorsque vous commencez à utiliser l’anneau contraceptif NuvaRing, il est recommandé d’utiliser des méthodes de contraception barrière supplémentaires pendant les sept premiers jours.
Avant d'utiliser l'anneau contraceptif pour la première fois, vous devez lire attentivement le mode d'emploi (il est bien sûr préférable de consulter votre médecin), car les conditions d'utilisation de l'anneau peuvent différer selon les cas.
Comment insérer l'anneau NuvaRing ?
 Pour insérer un anneau vaginal, une femme doit choisir une position confortable ; l'anneau peut être inséré en position debout, allongée ou accroupie.
Pour insérer un anneau vaginal, une femme doit choisir une position confortable ; l'anneau peut être inséré en position debout, allongée ou accroupie.
L’anneau doit être pressé et inséré dans le vagin, après quoi il prendra indépendamment la forme souhaitée, en fonction des caractéristiques individuelles de la structure de la femme.
Pour retirer l'anneau, vous devez le presser avec deux doigts (index et majeur) et le retirer du vagin.
Les saignements associés à l'arrêt du médicament commencent généralement 2 ou 3 jours après le retrait de l'anneau vaginal et peuvent ne s'arrêter qu'après l'insertion d'un nouvel anneau.
Les effets secondaires possibles
Malgré la libération locale d'hormones, des effets secondaires sont possibles lors de l'utilisation de NuvaRing.
Les femmes peuvent ressentir des maux de tête, des étourdissements, une instabilité émotionnelle (voire une dépression), une prise de poids, des troubles digestifs (nausées, vomissements, diarrhée), des pertes vaginales, des infections des voies génito-urinaires, une sensibilité des seins, etc.
Des réactions locales sont également possibles - sensation de corps étranger dans le vagin, inconfort lors des rapports sexuels.
Prix approximatif
L'anneau contraceptif NuvaRing est disponible en paquets de 1 anneau et de 3. Le prix moyen d'un paquet avec 1 anneau est de 30 $, un paquet de 3 anneaux est de 74 $.
Le choix de la méthode contraceptive est individuel pour chaque femme ; il est influencé par un certain nombre de facteurs, allant des caractéristiques de santé et physiologiques aux préférences personnelles.
Mais dans tous les cas, vous devez aborder ce choix en toute responsabilité, et il est conseillé de le faire non pas seul, mais avec un spécialiste compétent qui pourra prendre en compte non seulement vos souhaits, mais également les capacités de votre corps.
Contraceptif hormonal à usage intravaginal.Médicament : NuvaRing®
Substance active: éthinylestradiol, étonogestrel
Code ATX : G02BB01
KFG : Contraceptif hormonal pour administration intravaginale
Rég. numéro : P n° 015428/01
Date d'inscription : 25/12/03
Propriétaire enregistré. crédit.: ORGANON N.V. (Pays-Bas)
FORME POSOLOGIQUE, COMPOSITION ET CONDITIONNEMENT
Anneau vaginal lisse, transparente, incolore ou quasiment incolore, sans dommage visible majeur, avec une zone transparente ou quasi transparente à la jonction.
Excipients : copolymère d'éthylène-acétate de vinyle (28 % d'acétate de vinyle), copolymère d'éthylène-acétate de vinyle (9 % d'acétate de vinyle), stéarate de magnésium, eau purifiée.
1 PC. - un sac en aluminium (1) - des boîtes en carton.
La description du médicament NuvaRing est basée sur les instructions d'utilisation officiellement approuvées.
EFFET PHARMACHOLOGIQUE
Contraceptif hormonal à usage intravaginal contenant de l'œstrogène - éthinylestradiol et du gestagène - étonogestrel. L'étonogestrel, un dérivé de la 19-nortestostérone, se lie aux récepteurs de la progestérone dans les organes cibles.
L'effet contraceptif du médicament NuvaRing repose sur divers mécanismes, dont le plus important est l'inhibition de l'ovulation. L'indice de Pearl du médicament NuvaRing est de 0,765.
En plus de son effet contraceptif, le médicament NuvaRing a un effet positif sur le cycle menstruel. Avec son utilisation, le cycle devient plus régulier, les menstruations sont moins douloureuses, avec moins de saignements, ce qui peut contribuer à réduire la fréquence des carences en fer. De plus, il existe des preuves d’une réduction du risque de cancer de l’endomètre et des ovaires.
PHARMACOCINÉTIQUE
Étonogestrel
Succion
L'étonogestrel libéré par NuvaRing est rapidement absorbé par la muqueuse vaginale. La Cmax de l'étonogestrel d'environ 1 700 pg/ml est atteinte environ une semaine après l'insertion de l'anneau. Les concentrations sériques sont sujettes à de légères fluctuations et atteignent lentement un niveau de 1 400 pg/ml après 3 semaines. La biodisponibilité absolue est d'environ 100 %.
Distribution
L'étonogestrel se lie à l'albumine sérique et à la globuline liant les hormones sexuelles (SHBG). V d étonogestrel 2,3 l/kg.
Métabolisme
L'étonogestrel est métabolisé par hydroxylation et réduction pour former des conjugués sulfate et glucuronide. La clairance sérique est d'environ 3,5 l/h.
Suppression
La diminution des concentrations sériques d'étonogestrel est biphasique. La phase T1/2 ? dure environ 29 heures. L'étonogestrel et ses métabolites sont excrétés dans l'urine et la bile dans un rapport de 1,7 : 1. T 1/2 des métabolites est d'environ 6 jours.
Éthinylestradiol
Succion
L'éthinylestradiol libéré par NuvaRing est rapidement absorbé par la muqueuse vaginale. La Cmax est d'environ 35 pg/ml, atteinte 3 jours après l'insertion de l'anneau et diminue à 18 pg/ml après 3 semaines. La biodisponibilité absolue est d'environ 56 %, ce qui est comparable à la biodisponibilité orale.
Métabolisme
L'éthinylestradiol est initialement métabolisé par hydroxylation aromatique pour former une variété de métabolites hydroxylés et méthylés, qui sont présents à la fois à l'état libre et sous forme de conjugués glucuronide et sulfate. La clairance sérique est d'environ 3,5 l/h.
Suppression
La diminution de la concentration sérique d’éthinylestradiol est biphasique. La phase T1/2β est caractérisée par de grandes différences individuelles et dure en moyenne environ 34 heures. L'éthinylestradiol n'est pas excrété sous forme inchangée. ses métabolites sont excrétés dans l'urine et la bile dans un rapport de 1,3 : 1. La T1/2 des métabolites est d'environ 1,5 jours.
LES INDICATIONS
La contraception.
RÉGIME POSOLOGIQUE
NuvaRing est inséré dans le vagin une fois toutes les 4 semaines. L'anneau est placé dans le vagin pendant 3 semaines puis retiré le même jour de la semaine où il a été placé dans le vagin. Après une semaine de pause, un nouvel anneau est inséré. Les saignements associés à l'arrêt du médicament commencent généralement 2 à 3 jours après le retrait du NuvaRing et peuvent ne pas s'arrêter complètement jusqu'à ce que l'anneau suivant doive être utilisé.
Les contraceptifs hormonaux n'ont pas été utilisés au cours du cycle menstruel précédent
NuvaRing doit être administré entre le 1er et le 5ème jour du cycle menstruel, mais au plus tard le 5ème jour du cycle, même si la femme n'a pas terminé ses règles. Pendant les 7 premiers jours du premier cycle d'utilisation de NuvaRing, l'utilisation supplémentaire de méthodes de contraception barrière est recommandée.
Arrêter de prendre des contraceptifs oraux combinés
NuvaRing doit être administré au plus tard le lendemain de l’intervalle de prise du médicament. Si le contraceptif oral combiné contient également des comprimés inactifs (placebo), NuvaRing doit être administré au plus tard le lendemain de la prise du dernier comprimé placebo.
Passer d'une contraception progestative (mini-pilule, implant ou contraception injectable) ou d'un dispositif intra-utérin (DIU) libérant un progestatif
NuvaRing doit être administré n'importe quel jour (si le patient a pris des mini-pilules), le jour du retrait de l'implant ou du DIU et, avec une contraception injectable, le jour où la prochaine injection est nécessaire. Dans tous ces cas, une méthode de contraception barrière supplémentaire doit être utilisée pendant les 7 premiers jours d’utilisation de NuvaRing.
Après un avortement pratiqué au cours du premier trimestre de la grossesse
Vous pouvez commencer à utiliser NuvaRing immédiatement après un avortement. Dans ce cas, il n'est pas nécessaire d'utiliser d'autres contraceptifs. Si l'utilisation de NuvaRing immédiatement après un avortement n'est pas souhaitable, l'anneau doit être utilisé de la même manière que si des contraceptifs hormonaux n'avaient pas été utilisés au cours du cycle précédent.
Après un accouchement ou un avortement pratiqué au cours du deuxième trimestre de la grossesse
L'utilisation de NuvaRing doit commencer dans la 4ème semaine après l'accouchement ou l'avortement. Si l’utilisation de NuvaRing est commencée à une date ultérieure, l’utilisation supplémentaire de méthodes de contraception barrière est nécessaire au cours des 7 premiers jours d’utilisation de NuvaRing. Toutefois, si des rapports sexuels ont déjà eu lieu pendant cette période, vous devez d'abord exclure une grossesse ou attendre vos premières règles avant de commencer à utiliser NuvaRing.
L'effet contraceptif et le contrôle du cycle peuvent être altérés si la patiente ne respecte pas le régime recommandé. Pour éviter la perte de l'effet contraceptif en cas d'écart par rapport au régime, vous devez suivre les recommandations suivantes :
Quand interruption prolongée de l'utilisation de l'anneau Vous devez placer le nouvel anneau dans votre vagin dès que possible. De plus, au cours des 7 prochains jours, il est nécessaire d’utiliser une méthode de contraception barrière. Si vous avez eu des rapports sexuels pendant l’interruption de l’utilisation de l’anneau, vous devez envisager la possibilité d’une grossesse. Plus la pause est longue, plus le risque de grossesse est élevé.
Si l'anneau a été accidentellement retiré et est resté à l'extérieur du vaginmoins de 3 heures, l'effet contraceptif ne diminuera pas. L'anneau doit être réinséré dans le vagin dès que possible. Si l'anneau reste en dehors du vagin pendant plus de 3 heures, l'effet contraceptif peut être réduit. L'anneau doit être placé dans le vagin dès que possible, après quoi il doit rester dans le vagin de manière continue pendant au moins 7 jours, et une méthode de contraception barrière doit également être utilisée pendant ces 7 jours. Si l'anneau est resté hors du vagin pendant plus de 3 heures au cours de la troisième semaine d'utilisation, alors son utilisation doit être prolongée au-delà des trois semaines prescrites (jusqu'à la fin des 7 jours après la réinsertion de l'anneau). Après cela, l'anneau doit être retiré et un nouveau placé après une semaine de pause. Si l'anneau est retiré du vagin pendant plus de 3 heures au cours de la première semaine d'utilisation de l'anneau, la possibilité d'une grossesse doit être envisagée.
Quand anneau à usage prolongé, mais pas plus de 4 semaines, l'effet contraceptif persiste. Vous pouvez faire une pause d'une semaine puis placer une nouvelle bague. Si NuvaRing est resté dans le vagin pendant plus de 4 semaines, l'effet contraceptif peut diminuer et une grossesse doit être exclue avant d'utiliser un nouvel anneau NuvaRing.
Si la patiente ne respecte pas le régime recommandé et ne présente pas de saignement causé par le retrait de l'anneau pendant une semaine d'arrêt de l'utilisation de l'anneau, une grossesse doit être exclue avant d'utiliser un nouvel anneau vaginal.
À retarder l'apparition des règles, vous pouvez commencer à utiliser la nouvelle bague sans une semaine de pause. L'anneau suivant doit également être utilisé pendant 3 semaines. Cela peut provoquer des saignements ou des spottings. Ensuite, après la pause requise d’une semaine, vous devez reprendre une utilisation régulière de NuvaRing.
Pour décaler le début des règles à un autre jour de la semaine à partir du jour qui tombe selon le schéma actuel d'utilisation de l'anneau, vous pouvez raccourcir la prochaine interruption d'utilisation de l'anneau d'autant de jours que nécessaire. Plus la pause d'utilisation de l'anneau est courte, plus la probabilité qu'aucun saignement ne se produise après le retrait de l'anneau et que l'apparition de saignements ou de spottings intempestifs lors de l'utilisation de l'anneau suivant est élevée.
Règles d'utilisation de NuvaRing
La patiente peut insérer indépendamment NuvaRing dans le vagin. Pour insérer l'anneau, une femme doit choisir la position qui lui est la plus confortable, par exemple debout, lever une jambe, s'accroupir ou s'allonger. NuvaRing doit être pressé et inséré dans le vagin jusqu'à ce que l'anneau soit dans une position confortable. La position exacte de NuvaRing dans le vagin n’est pas déterminante pour l’effet contraceptif de l’anneau.
Après insertion, l’anneau doit rester continuellement dans le vagin pendant 3 semaines. S'il est accidentellement retiré (par exemple lors du retrait d'un tampon), l'anneau doit être rincé à l'eau tiède et immédiatement placé dans le vagin. Pour retirer l'anneau, vous pouvez le saisir avec votre index ou le serrer entre votre index et votre majeur et le retirer du vagin.
EFFETS SECONDAIRES de NuvaRing
Du côté du système nerveux central : maux de tête, migraine, dépression, instabilité émotionnelle, étourdissements, anxiété, sensation de fatigue.
Du système digestif : nausées, douleurs abdominales, diarrhée, vomissements, diminution de la libido.
Du système endocrinien : augmentation ou diminution du poids corporel.
Du système reproducteur : pertes vaginales (« leucorrhée »), vaginite, cervicite, douleur, tension et hypertrophie des glandes mammaires, dysménorrhée.
Du système urinaire : infections des voies urinaires (y compris la cystite).
Réactions locales : prolapsus de l'anneau, sensation d'inconfort lors des rapports sexuels chez la femme et l'homme, sensation de corps étranger dans le vagin.
CONTRE-INDICATIONS
Thrombose/thromboembolie veineuse ou artérielle (y compris des antécédents) ;
Facteurs de risque de thrombose (y compris les antécédents) ;
Migraine avec symptômes neurologiques focaux ;
Angiopathie diabétique ;
Pancréatite (y compris des antécédents) associée à un degré élevé d'hypertriglycéridémie (concentration de LDL supérieure à 500 mg/dl) ;
Maladies hépatiques graves (jusqu'à normalisation des indicateurs fonctionnels);
Tumeurs hépatiques (bénignes ou malignes, y compris les antécédents) ;
Tumeurs malignes hormono-dépendantes (établies ou suspectées, par exemple tumeurs des organes génitaux ou des glandes mammaires) ;
Saignement vaginal d'étiologie inconnue ;
Grossesse ou suspicion de celle-ci ;
Période de lactation ;
Hypersensibilité aux composants du médicament.
AVEC prudence le médicament doit être prescrit dans le diabète sucré, l'obésité (indice de masse corporelle supérieur à 30 kg/m2), l'hypertension artérielle, la fibrillation auriculaire, la valvulopathie cardiaque, la dyslipoprotéinémie, les maladies du foie ou de la vésicule biliaire, la maladie de Crohn ou la colite ulcéreuse, la drépanocytose, le LED, syndrome hémolytique et urémique, épilepsie, tabagisme en association avec un âge supérieur à 35 ans, avec immobilisation prolongée, interventions chirurgicales majeures, mastopathie fibrokystique, fibromes utérins, hyperbilirubinémie congénitale (syndrome de Gilbert, Dubin-Johnson et Rotor), chloasma (éviter l'exposition aux rayons ultraviolets) , ainsi que les conditions rendant difficile l'utilisation d'un anneau vaginal (prolapsus cervical, hernie vésicale, hernie rectale, constipation chronique sévère).
GROSSESSE ET ALLAITEMENT
L'utilisation de NuvaRing est contre-indiquée pendant la grossesse, les suspicions de grossesse et l'allaitement.
INSTRUCTIONS SPÉCIALES
Avant de prescrire NuvaRing, vous devez recueillir les antécédents médicaux détaillés du patient et procéder à un examen médical, en tenant compte des contre-indications et des précautions. Pendant la période d'utilisation de NuvaRing, l'examen doit être répété au moins une fois par an. La fréquence et la liste des études doivent être sélectionnées individuellement pour chaque patiente, mais dans tous les cas, une attention particulière doit être accordée au contrôle de la pression artérielle, à l'examen des glandes mammaires, des organes abdominaux et pelviens, y compris l'examen cytologique du col de l'utérus et les tests de laboratoire pertinents. .
L'efficacité de NuvaRing peut être réduite si le régime n'est pas suivi ou si d'autres médicaments sont utilisés de manière concomitante.
S'il est nécessaire d'utiliser des médicaments susceptibles d'affecter l'effet contraceptif de l'anneau pendant l'utilisation de NuvaRing, vous devez utiliser une méthode de contraception barrière en plus d'utiliser NuvaRing ou choisir une autre méthode de contraception. Lorsque vous prenez des inducteurs d'enzymes hépatiques microsomales pendant l'utilisation de NuvaRing, vous devez utiliser une méthode de contraception barrière pendant la prise de médicaments concomitants et pendant 28 jours après leur arrêt. Lors de la prise simultanée d'antibiotiques (à l'exclusion de la rifampicine et de la griséofulvine), la méthode barrière doit être utilisée pendant au moins 7 jours après l'arrêt du traitement antibactérien. Si le traitement avec des médicaments concomitants se poursuit au-delà de 3 semaines d'utilisation de l'anneau, l'anneau suivant est placé immédiatement, sans interruption d'une semaine.
L'utilisation de stéroïdes contraceptifs peut affecter les résultats de certains tests de laboratoire, notamment les paramètres biochimiques de la fonction hépatique, thyroïdienne, surrénale et rénale, les taux plasmatiques de protéines de transport (par exemple, la globuline liant les corticostéroïdes et la globuline liant les hormones sexuelles), les fractions lipidiques/lipoprotéiques. , paramètres du métabolisme des glucides et indicateurs de la coagulation et de la fibrinolyse. En règle générale, les indicateurs varient dans les limites des valeurs normales.
Pendant la grossesse ou la prise de contraceptifs hormonaux oraux, des affections telles que l'herpès gestationnel, la perte auditive, la chorée de Sydenham (chorée mineure) et la porphyrie peuvent survenir.
Le patient doit être informé que NuvaRing ne protège pas contre l'infection par le VIH (SIDA) et d'autres maladies sexuellement transmissibles.
Lors de l'utilisation de NuvaRing, des saignements irréguliers peuvent survenir (écoulement mineur ou saignement soudain).
Certaines femmes ne présentent aucun saignement causé par le retrait de l’anneau lorsqu’elles ne l’utilisent pas. Si NuvaRing est utilisé conformément aux instructions, il est peu probable que la femme soit enceinte. Si vous vous écartez du régime recommandé et qu'il n'y a pas de saignement dû à l'arrêt du médicament, ou s'il n'y a pas de saignement 2 fois de suite, une grossesse doit être exclue.
L'étendue de l'exposition et les effets pharmacologiques possibles de l'éthinylestradiol et de l'étonogestrel sur les partenaires sexuels par absorption par la peau du pénis n'ont pas été étudiés.
SURDOSAGE
Les cas de surdosage sont inconnus.
Allégué symptômes: nausées, vomissements, saignements vaginaux.
Traitement: effectuer un traitement symptomatique. Il n’existe pas d’antidote.
INTERACTIONS MÉDICAMENTEUSES
Les interactions entre les contraceptifs hormonaux et d'autres médicaments peuvent entraîner des saignements intermenstruels et/ou une perte de l'effet contraceptif.
Avec l'utilisation simultanée de NuvaRing avec des médicaments induisant des enzymes hépatiques microsomales (phénytoïne, phénobarbital, primidone, carbamazépine, rifampicine, oxcarbazépine, topiramate, felbamate, ritonavir, griséofulvine, millepertuis), le métabolisme des hormones sexuelles est augmenté et l'effet contraceptif de NuvaRing est réduite.
L'efficacité de NuvaRing peut également être réduite lors de la prise simultanée de certains antibiotiques, tels que les pénicillines et les tétracyclines. Ces médicaments réduisent la circulation entérohépatique des œstrogènes, entraînant une diminution des concentrations d'éthinylestradiol.
L'effet sur l'effet contraceptif et la sécurité de NuvaRing des médicaments antifongiques et des spermicides prescrits par voie intravaginale est inconnu.
Aucune interaction directe n'a été observée entre l'étonogestrel et l'éthinylestradiol co-administré.
CONDITIONS DE VACANCES EN PHARMACIE
Le médicament NuvaRing est disponible sur ordonnance.
CONDITIONS ET DURÉE DE STOCKAGE
NuvaRing doit être conservé hors de la portée des enfants, à une température comprise entre 2° et 8°C. Durée de conservation - 3 ans.
Catad_pgroup Contraceptifs locaux
Indications pour l'utilisation
- La contraception
- Ménorragie idiopathique
- Prévention de l'hyperplasie de l'endomètre pendant le THS
LES INFORMATIONS SONT FOURNIES STRICTEMENT
POUR LES PROFESSIONNELS DE LA SANTÉ
NuvaRing - mode d'emploi officiel*
*enregistré par le ministère de la Santé de la Fédération de Russie (selon grls.rosminzdrav.ru)
INSTRUCTIONS
sur l'utilisation d'un médicament à usage médical
Numéro d'enregistrement :
Nom commercial :
NuvaRing®
Dénomination commune internationale ou nom générique :
éthinylestradiol + étonogestrel
Forme posologique :
anneaux vaginaux
Composé
1 anneau vaginal contient :
substances actives :étonogestrel – 11,7 mg, éthinylestradiol – 2,7 mg ;
Excipients : Copolymère d'éthylène et d'acétate de vinyle – 1677 mg, copolymère d'éthylène et d'acétate de vinyle – 197 mg, stéarate de magnésium – 1,7 mg.
Description
Un anneau lisse, transparent, incolore ou quasiment incolore sans dommage visible majeur avec une zone transparente ou quasi transparente à la jonction.
Groupe pharmacothérapeutique :
contraceptif combiné (œstrogène + gestagène)
Code ATX: G02BB01
Propriétés pharmacologiques
Pharmacodynamie
Mécanisme d'action
Le médicament NuvaRing ® est un contraceptif hormonal combiné contenant de l'étonogestrel et de l'éthinylestradiol. L'étonogestrel est un progestatif (dérivé de la 19-nortestostérone) qui se lie avec une forte affinité aux récepteurs de la progestérone dans les organes cibles. L'éthinylestradiol est un œstrogène largement utilisé dans la production de contraceptifs.
L'effet contraceptif du médicament NuvaRing ® est dû à une combinaison de divers facteurs, dont le plus important est la suppression de l'ovulation.
Efficacité
Dans les études cliniques, il a été constaté que l'indice de Pearl (un indicateur reflétant l'incidence des grossesses chez 100 femmes pendant 1 an de contraception) chez les femmes âgées de 18 à 40 ans pour le médicament NuvaRing ® était de 0,96 (IC à 95 % : 0,64 -1,39). ) et 0,64 (IC à 95 % : 0,35-1,07) dans l'analyse statistique de tous les participants randomisés (analyse ITT) et dans l'analyse des participants à l'étude qui ont terminé l'étude selon le protocole (analyse PP), respectivement. Ces valeurs étaient similaires aux valeurs de l'indice de Pearl obtenues dans des études comparatives de contraceptifs oraux combinés (COC) contenant du lévonorgestrel/éthinylestradiol (0,150/0,030 mg) ou de la drospirénone/éthinylestradiol (3/0,30 mg).
Avec l'utilisation du médicament NuvaRing ®, le cycle devient plus régulier, la douleur et l'intensité des saignements de type menstruel diminuent, ce qui contribue à réduire l'incidence des carences en fer. Il existe des preuves d'une réduction du risque de cancer de l'endomètre et des ovaires grâce à l'utilisation de ce médicament.
Nature du saignement
Une comparaison des schémas de saignements sur un an chez 1 000 femmes utilisant le médicament NuvaRing ® et des COC contenant du lévonorgestrel/éthinylestradiol (0,150/0,030 mg) a montré une réduction significative de la fréquence des saignements intermenstruels ou des microrragies lors de l'utilisation du médicament NuvaRing ® par rapport à COOK. . De plus, la fréquence des cas de saignements survenus uniquement pendant une interruption de l'utilisation du médicament était significativement plus élevée chez les femmes utilisant le médicament NuvaRing ® .
Effet sur la densité minérale osseuse
Une étude comparative de deux ans de l'effet du médicament NuvaRing ® (n = 76) et d'un dispositif intra-utérin non hormonal (n = 31) n'a révélé aucun effet sur la densité minérale osseuse chez les femmes.
Enfants
L'innocuité et l'efficacité de NuvaRing ® chez les adolescentes de moins de 18 ans n'ont pas été étudiées.
Pharmacocinétique
Étonogestrel
Succion
L'étonogestrel, libéré par l'anneau vaginal NuvaRing ®, est rapidement absorbé par la muqueuse vaginale. La concentration maximale d'étonogestrel dans le plasma sanguin, d'environ 1 700 pg/ml, est atteinte environ 1 semaine après l'insertion de l'anneau. Les concentrations plasmatiques varient dans une petite plage et diminuent lentement jusqu'à environ 1 600 pg/ml après 1 semaine, 1 500 pg/ml après 2 semaines et 1 400 pg/ml après 3 semaines d'utilisation. La biodisponibilité absolue est d'environ 100 %, ce qui dépasse la biodisponibilité de l'étonogestrel pris par voie orale. Sur la base des résultats des mesures des concentrations d'étonogestrel dans le col de l'utérus et à l'intérieur de l'utérus chez les femmes utilisant le médicament NuvaRing ® et les femmes utilisant des contraceptifs oraux contenant 0,150 mg de désogestrel et 0,020 mg d'éthinylestradiol, les valeurs observées des concentrations d'étonogestrel étaient comparables. .
Distribution
L'étonogestrel se lie à l'albumine plasmatique et à la globuline liant les hormones sexuelles (SHBG). Le volume apparent de distribution de l'étonogestrel est de 2,3 L/kg.
Métabolisme
La biotransformation de l'étonogestrel se produit par des voies connues du métabolisme des hormones sexuelles. La clairance apparente du plasma sanguin est d'environ 3,5 l/h. Aucune interaction directe avec l'éthinylestradiol pris en concomitance n'a été identifiée.
Suppression
Les concentrations plasmatiques d'étonogestrel diminuent en deux phases. En phase terminale, la demi-vie est d'environ 29 heures et ses métabolites sont excrétés par les reins et par les intestins avec la bile dans un rapport d'environ 1,7:1. La demi-vie des métabolites est d'environ 6 jours.
Éthinylestradiol
Succion
L'éthinylestradiol, libéré par l'anneau vaginal NuvaRing ®, est rapidement absorbé par la muqueuse vaginale. La concentration plasmatique maximale d'environ 35 pg/ml est atteinte 3 jours après l'administration de l'anneau et diminue à 19 pg/ml après 1 semaine, à 18 pg/ml après 2 semaines et 18 pg/ml après 3 semaines d'utilisation. La biodisponibilité absolue est d'environ 56 % et est comparable à celle de l'éthinylestradiol oral. Sur la base des résultats des mesures des concentrations d'éthinylestradiol dans le col de l'utérus et à l'intérieur de l'utérus chez les femmes utilisant le médicament NuvaRing ® et les femmes utilisant des contraceptifs oraux contenant 0,150 mg de désogestrel et 0,020 mg d'éthinylestradiol, les valeurs observées des concentrations d'éthinylestradiol étaient comparables.
Les concentrations d'éthinylestradiol ont été étudiées dans une étude randomisée comparative de NovaRing ® (libération vaginale quotidienne d'éthinylestradiol 0,015 mg), d'un dispositif transdermique (norelgestromine/éthinylestradiol ; libération quotidienne d'éthinylestradiol 0,020 mg) et de COC (lévonorgestrel/éthinylestradiol ; libération quotidienne). d'éthinylestradiol 0,030 mg) au cours d'un cycle chez des femmes en bonne santé. L'exposition systémique à l'éthinylestradiol au cours d'un mois (ASC0-?) pour le médicament NuvaRing ® était statistiquement significativement inférieure à celle du patch et des COC et s'élevait respectivement à 10,9, 37,4 et 22,5 ng h/ml.
Distribution
L'éthinylestradiol se lie de manière non spécifique à l'albumine plasmatique. Le volume apparent de distribution est d'environ 15 l/kg.
Métabolisme
L'éthinylestradiol est métabolisé par hydroxylation aromatique. Lors de sa biotransformation, un grand nombre de métabolites hydroxylés et méthylés se forment. Ils circulent librement ou sous forme de conjugués sulfate et glucuronide. Le jeu apparent est d'environ 35 l/h.
Suppression
Les concentrations plasmatiques d'éthinylestradiol diminuent en deux phases. La demi-vie en phase terminale varie considérablement ; la durée médiane est d'environ 34 heures. L'éthinylestradiol n'est pas excrété sous forme inchangée. Les métabolites de l'éthinylestradiol sont excrétés par les reins et par les intestins avec la bile dans un rapport de 1,3:1. La demi-vie des métabolites est d'environ 1,5 jour.
Groupes de patients spéciaux
Enfants
La pharmacocinétique de NovaRing ® chez les adolescentes en bonne santé de moins de 18 ans ayant déjà leurs règles n'a pas été étudiée.
Dysfonctionnement rénal
L'effet de la maladie rénale sur la pharmacocinétique de NovaRing ® n'a pas été étudié.
Dysfonctionnement hépatique
L'effet des maladies hépatiques sur la pharmacocinétique de NovaRing ® n'a pas été étudié. Cependant, chez les patients présentant une insuffisance hépatique, le métabolisme des hormones sexuelles peut se détériorer.
Groupes ethniques
La pharmacocinétique du médicament chez les représentants de groupes ethniques n'a pas été spécifiquement étudiée.
Indications pour l'utilisation
La contraception.
Contre-indications
Le médicament NuvaRing ® est contre-indiqué en présence de l'une des conditions énumérées ci-dessous. Si l'une de ces conditions survient pendant l'utilisation du médicament NuvaRing ®, vous devez immédiatement arrêter d'utiliser le médicament.
- Thrombose (artérielle ou veineuse) et thromboembolie actuelle ou antérieure (y compris thrombose veineuse profonde, embolie pulmonaire, infarctus du myocarde, troubles cérébrovasculaires).
- Conditions précédant une thrombose (y compris les accidents ischémiques transitoires, l'angine de poitrine) actuellement ou dans le passé.
- Prédisposition au développement de thromboses veineuses ou artérielles, y compris maladies héréditaires : résistance à la protéine C activée, déficit en antithrombine III, déficit en protéine C, déficit en protéine S, hyperhomocystéinémie et anticorps antiphospholipides (anticorps anticardiolipine, anticoagulant lupique).
- Migraine avec symptômes neurologiques focaux actuels ou antérieurs.
- Diabète sucré avec lésions vasculaires.
- Facteurs de risque sévères ou multiples de thrombose veineuse ou artérielle : prédisposition héréditaire à la thrombose (thrombose, infarctus du myocarde ou accident vasculaire cérébral à un jeune âge chez un membre de la famille immédiate), hypertension, lésions de l'appareil valvulaire du cœur, fibrillation auriculaire, étendue intervention chirurgicale, immobilisation prolongée, traumatisme étendu, obésité (poids corporel > 30 kg/m²), tabagisme chez la femme de plus de 35 ans (voir rubrique « Instructions particulières »).
- Pancréatite avec hypertriglycéridémie sévère, actuelle ou historique.
- Maladies hépatiques graves.
- Tumeurs hépatiques (malignes ou bénignes), y compris les antécédents.
- Tumeurs malignes hormono-dépendantes connues ou suspectées (par exemple génitales ou mammaires).
- Saignement du vagin d'étiologie inconnue.
- Grossesse, y compris suspicion de grossesse.
- Hypersensibilité à l'un des actifs ou excipients du médicament NuvaRing ®.
Soigneusement
Si l'une des maladies, affections ou facteurs de risque énumérés ci-dessous est présente, les avantages de l'utilisation du médicament NuvaRing ® et les risques possibles pour chaque femme doivent être évalués avant qu'elle ne commence à utiliser le médicament NuvaRing ® (voir la section « Instructions spéciales »). . En cas d'exacerbation de maladies, de détérioration de l'état ou de première apparition de l'une des affections énumérées ci-dessous, une femme doit consulter un médecin pour décider de la possibilité d'une utilisation ultérieure du médicament NuvaRing ®.
Le médicament NuvaRing ® doit être utilisé avec prudence dans les cas suivants :
- facteurs de risque de développement d'une thrombose et d'une thromboembolie : prédisposition héréditaire à la thrombose (thrombose, infarctus du myocarde ou accident vasculaire cérébral à un jeune âge dans l'un des membres de la famille immédiate), tabagisme, obésité, dyslipoprotéinémie, hypertension artérielle, migraine sans symptômes neurologiques focaux, cœur maladie valvulaire , troubles du rythme cardiaque, immobilisation prolongée, interventions chirurgicales graves ;
- thrombophlébite des veines superficielles;
- dyslipoprotéinémie;
- maladie des valvules cardiaques;
- hypertension artérielle correctement contrôlée ;
- diabète sucré sans complications vasculaires;
- maladies hépatiques aiguës ou chroniques;
- jaunisse et/ou démangeaisons causées par une cholestase ;
- lithiase biliaire;
- porphyrie;
- le lupus érythémateux disséminé;
- Syndrome hémolytique urémique;
- Chorée de Sydenham (chorée mineure) ;
- perte auditive due à l'otospongiose;
- (héréditaire) angio-œdème ;
- maladies inflammatoires chroniques de l'intestin (maladie de Crohn et colite ulcéreuse) ;
- l'anémie falciforme;
- chloasma;
- Conditions pouvant rendre difficile l'utilisation d'un anneau vaginal : prolapsus cervical, hernie vésicale, hernie rectale, constipation chronique sévère.
Utilisation pendant la grossesse et l'allaitement
Le médicament NuvaRing ® est destiné à prévenir la grossesse. Si une femme souhaite arrêter d'utiliser le médicament afin de tomber enceinte, il est recommandé d'attendre le rétablissement du cycle naturel pour concevoir, car cela aidera à calculer correctement la date de conception et d'accouchement.
Grossesse
L'utilisation de NuvaRing ® pendant la grossesse est contre-indiquée. En cas de grossesse, l'anneau doit être retiré. Des études épidémiologiques approfondies n'ont pas révélé de risque accru de malformations congénitales chez les enfants nés de femmes ayant pris des COC avant la grossesse, ni d'effets tératogènes dans les cas où les femmes prenaient des COC en début de grossesse sans le savoir. Bien que cela s'applique à tous les COC, on ne sait pas si cela s'applique également à NuvaRing ® . Une étude clinique menée auprès d'un petit groupe de femmes a montré que, malgré le fait que le médicament NuvaRing ® soit administré dans le vagin, les concentrations d'hormones sexuelles contraceptives à l'intérieur de l'utérus lors de l'utilisation du médicament NuvaRing ® sont similaires à celles lors de l'utilisation de COC. Les issues de grossesse chez les femmes qui ont utilisé NuvaRing ® au cours d'un essai clinique n'ont pas été décrites.
Période d'allaitement
L'utilisation de NuvaRing ® pendant l'allaitement n'est pas indiquée. La composition du médicament peut affecter la lactation, réduire la quantité et modifier la composition du lait maternel. De petites quantités d'hormones sexuelles contraceptives et/ou de leurs métabolites peuvent être excrétées dans le lait, mais il n'existe aucune preuve de leur impact négatif sur la santé des enfants.
Conseil d'utilisation et doses
Pour obtenir un effet contraceptif, le médicament NuvaRing ® doit être utilisé conformément aux instructions.
Une femme peut insérer indépendamment l'anneau vaginal NuvaRing ® dans le vagin.
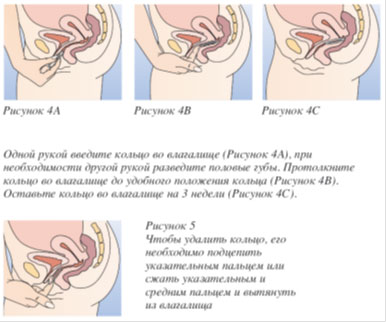
Le médecin doit expliquer à la femme comment insérer et retirer l'anneau vaginal NuvaRing ®. Pour insérer l'anneau, la femme doit choisir une position confortable, par exemple debout, lever une jambe, accroupie ou allongée. L'anneau vaginal NuvaRing ® doit être pressé et inséré dans le vagin jusqu'à ce qu'il soit dans une position confortable. La position exacte de l'anneau dans le vagin n'est pas déterminante pour l'effet contraceptif (Fig. 1-4).
Après l'administration (voir la sous-section « Comment commencer à utiliser le médicament NuvaRing ® »), l'anneau doit rester continuellement dans le vagin pendant 3 semaines. Il est conseillé à une femme de vérifier régulièrement s'il reste dans le vagin. Si l'anneau a été retiré accidentellement, vous devez suivre les instructions de la sous-section « Que faire si l'anneau a été temporairement retiré du vagin ».
L'anneau vaginal NuvaRing ® doit être retiré après 3 semaines, le même jour de la semaine où l'anneau a été inséré dans le vagin. Après une semaine de pause, un nouvel anneau est inséré (par exemple, si l'anneau vaginal NuvaRing ® a été installé mercredi vers 22h00, il doit être retiré mercredi 3 semaines plus tard vers 22h00. Un nouvel anneau est inséré le mercredi suivant). Pour retirer l'anneau, vous devez le saisir avec votre index ou le presser avec votre index et votre majeur et le retirer du vagin (Fig. 5). L'anneau usagé doit être placé dans un sac (conserver hors de portée des enfants et des animaux domestiques) et jeté. Les saignements associés à l'arrêt de l'action du médicament NuvaRing ® commencent généralement 2 à 3 jours après le retrait de l'anneau vaginal NovaRing ® et peuvent ne pas s'arrêter complètement jusqu'à l'installation d'un nouvel anneau.

Comment commencer à utiliser le médicament NuvaRing ® ?
- Les contraceptifs hormonaux n'ont pas été utilisés lors du cycle précédent
Le médicament NuvaRing ® doit être administré le premier jour du cycle (c'est-à-dire le premier jour des règles). Il est possible d'installer un anneau les jours 2 à 5 du cycle, cependant, au cours du premier cycle au cours des 7 premiers jours d'utilisation du médicament NuvaRing ®, l'utilisation supplémentaire de méthodes de contraception barrière est recommandée. - Passer des contraceptifs hormonaux combinés
Une femme doit insérer l'anneau vaginal NuvaRing ® le dernier jour de l'intervalle habituel entre les cycles lorsqu'elle prend des contraceptifs hormonaux combinés (pilules ou patch).
Si une femme a pris correctement et régulièrement un contraceptif hormonal combiné et est sûre de ne pas être enceinte, elle peut passer à l'utilisation d'un anneau vaginal n'importe quel jour du cycle.
En aucun cas vous ne devez dépasser l’intervalle sans hormones recommandé par la méthode précédente. - Passer des médicaments uniquement progestatifs (mini-pilules, contraceptifs oraux progestatifs seuls, implants, injectables ou systèmes intra-utérins (DIU) contenant des hormones)
Une femme qui prend des mini-pilules ou des contraceptifs oraux progestatifs peut passer à NuvaRing ® n'importe quel jour. L'anneau est posé le jour du retrait de l'implant ou du DIU. Si une femme a reçu des injections, l'utilisation du médicament NuvaRing ® commence le jour où la prochaine injection aurait dû être administrée. Dans tous ces cas, la femme doit utiliser une méthode contraceptive barrière pendant les 7 premiers jours après l’insertion de l’anneau. - Après un avortement au premier trimestre
Une femme peut insérer l'anneau immédiatement après un avortement. Dans ce cas, elle n’a pas besoin de contraceptifs supplémentaires. Si l'utilisation du médicament NuvaRing ® immédiatement après un avortement n'est pas souhaitable, il est nécessaire de suivre les recommandations données dans la sous-section «Au cours du cycle précédent, aucun contraceptif hormonal n'a été utilisé». Entre-temps, il est recommandé à la femme une méthode alternative de contraception. - Après un accouchement ou après un avortement au deuxième trimestre
Il est conseillé à une femme de faire insérer l'anneau au plus tôt 4 semaines après l'accouchement (si elle n'allaite pas) ou après un avortement au deuxième trimestre. Si l’anneau est installé ultérieurement, il est recommandé d’utiliser une méthode barrière supplémentaire pendant les 7 premiers jours. Cependant, si un rapport sexuel a déjà eu lieu, avant d'utiliser le médicament NuvaRing ®, il est nécessaire d'exclure une grossesse ou d'attendre la première menstruation.
L'effet contraceptif et le contrôle du cycle peuvent être altérés si une femme ne respecte pas le régime recommandé. Pour éviter une diminution de l'effet contraceptif, les recommandations suivantes doivent être suivies.
- Que faire si l'interruption d'utilisation de l'anneau se prolonge ?
Si vous avez eu des rapports sexuels pendant une pause dans l'utilisation de l'anneau, une grossesse doit être exclue. Plus la pause est longue, plus le risque de grossesse est élevé. Si une grossesse est exclue, la femme doit insérer un nouvel anneau dans le vagin le plus rapidement possible. Au cours des 7 prochains jours, une méthode de contraception barrière supplémentaire, comme un préservatif, doit être utilisée. - Que faire si l'anneau a été temporairement retiré du vagin ?
L'anneau doit rester dans le vagin en continu pendant 3 semaines. Si l'anneau a été accidentellement retiré, il doit être lavé à l'eau froide ou légèrement tiède (pas chaude) et immédiatement inséré dans le vagin.- Si l’anneau reste hors du vagin moins de 3 heures, son effet contraceptif n’est pas réduit. La femme doit insérer l'anneau dans le vagin le plus rapidement possible (au plus tard après 3 heures).
- Si l'anneau est resté hors du vagin pendant plus de 3 heures au cours de la première ou de la deuxième semaine d'utilisation, l'effet contraceptif peut être réduit. Une femme doit insérer l'anneau dans son vagin le plus rapidement possible. Au cours des 7 prochains jours, vous devez utiliser une méthode de contraception barrière, comme un préservatif. Plus l'anneau est resté longtemps en dehors du vagin et plus cette période est proche de l'interruption de 7 jours de l'utilisation de l'anneau, plus le risque de grossesse est élevé.
- Si l'anneau est resté hors du vagin pendant plus de 3 heures au cours de la troisième semaine d'utilisation, l'effet contraceptif peut être réduit. La femme doit jeter la bague et choisir l’une des deux méthodes suivantes.
- Installez immédiatement un nouvel anneau.
Note: la nouvelle bague peut être utilisée pendant les 3 prochaines semaines. Dans ce cas, il ne peut y avoir aucun saignement associé à l’arrêt du médicament. Cependant, des spottings ou des saignements en milieu de cycle sont possibles. - Attendez les saignements liés à l'arrêt du médicament et insérez un nouvel anneau au plus tard 7 jours après avoir retiré l'anneau précédent.
Note: Cette option ne doit être choisie que si le schéma d'application en anneau n'a pas été violé au cours des deux premières semaines.
- Installez immédiatement un nouvel anneau.
- Que faire en cas d'utilisation prolongée de la bague ?
Si le médicament NuvaRing ® n'a pas été utilisé pendant une période maximale de 4 semaines, l'effet contraceptif reste suffisant. Une femme peut prendre une semaine de pause sans utiliser l'anneau, puis insérer un nouvel anneau.
Si l'anneau vaginal NuvaRing ® reste dans le vagin pendant plus de 4 semaines, l'effet contraceptif peut s'aggraver, c'est pourquoi une grossesse doit être exclue avant d'insérer un nouvel anneau.
Si une femme ne respecte pas le régime recommandé et qu'aucun saignement ne survient après une semaine d'interruption de l'utilisation de l'anneau, une grossesse doit être exclue avant d'introduire un nouvel anneau. - Comment décaler ou retarder l’apparition des saignements menstruels ?
Pour retarder les saignements de privation de type menstruel, une femme peut insérer un nouvel anneau sans une semaine de pause. L'anneau suivant doit être utilisé pendant 3 semaines. Cela peut provoquer des saignements ou des saignements. Ensuite, après la pause habituelle d'une semaine, la femme reprend une utilisation régulière du médicament NuvaRing ® .
Pour reporter l'apparition des saignements à un autre jour de la semaine, il peut être conseillé à la femme de prendre une pause plus courte dans l'utilisation de l'anneau (autant de jours que nécessaire). Plus la pause d'utilisation de l'anneau est courte, plus la probabilité qu'aucun saignement ne se produise après le retrait de l'anneau et que des saignements ou des saignements se produisent lors de l'utilisation de l'anneau suivant est élevée.
Enfants
L'innocuité et l'efficacité de NuvaRing ® chez les adolescentes de moins de 18 ans n'ont pas été étudiées.
Effet secondaire
Lors de l'utilisation du médicament, des effets secondaires peuvent survenir, à des fréquences variables : souvent (?1/100), rarement (<1/100, ?1/1 000), редко (<1/1 000, ?1/10 000).
Les conséquences graves d'un surdosage de contraceptifs hormonaux n'ont pas été décrites. Les symptômes possibles comprennent des nausées, des vomissements et de légers saignements vaginaux chez les jeunes filles. Il n’existe pas d’antidote. Le traitement est symptomatique.
Interactions avec d'autres médicaments et autres types d'interactions
Interaction avec d'autres médicaments
Les interactions entre les contraceptifs hormonaux et d'autres médicaments peuvent entraîner l'apparition de saignements acycliques et/ou un échec de la contraception.
La littérature décrit les interactions suivantes avec les contraceptifs oraux combinés en général.
Métabolisme hépatique : des interactions peuvent survenir avec des médicaments qui induisent des enzymes microsomales hépatiques, ce qui peut entraîner une augmentation de la clairance des hormones sexuelles. Des interactions ont été établies par exemple avec la phénytoïne, les barbituriques, la primidone, la carbamazépine, la rifampicine, ainsi qu'éventuellement avec l'oxcarbazépine, le topiramate, le felbamate, le ritonavir, la griséofulvine et les préparations contenant du millepertuis (Hypericum perforatum).
Lors du traitement avec l'un des médicaments répertoriés, vous devez utiliser temporairement une méthode de contraception barrière (préservatif) en association avec l'utilisation du médicament NuvaRing ® ou choisir une autre méthode de contraception. Lors de l'utilisation concomitante de médicaments induisant des enzymes microsomales et pendant 28 jours après leur arrêt, des méthodes de contraception barrière doivent être utilisées.
Si le traitement concomitant doit être poursuivi après 3 semaines d'utilisation de l'anneau, l'anneau suivant doit être administré immédiatement, sans respecter l'intervalle habituel.
Antibiotiques : une diminution de l'efficacité des contraceptifs oraux contenant de l'éthinylestradiol a été observée avec l'utilisation concomitante d'antibiotiques tels que l'ampicilline et les tétracyclines. Le mécanisme de cet effet n’a pas été étudié. Dans une étude d'interaction pharmacocinétique, l'administration orale d'amoxicilline (875 mg, 2 fois par jour) ou de doxycycline (200 mg par jour, puis 100 mg par jour) pendant 10 jours lors de l'utilisation de NovaRing ® a eu peu d'effet sur la pharmacocinétique de l'étonogestrel et de l'éthinylestradiol. Lors de l'utilisation d'antibiotiques (à l'exclusion de l'amoxicilline et de la doxycycline), vous devez utiliser une méthode de contraception barrière (préservatif) pendant le traitement et pendant 7 jours après l'arrêt des antibiotiques. Si le traitement concomitant doit être poursuivi après 3 semaines d'utilisation de l'anneau, l'anneau suivant doit être administré immédiatement, sans respecter l'intervalle habituel.
Les études pharmacocinétiques n'ont pas révélé l'effet de l'utilisation simultanée d'agents antifongiques et de spermicides sur l'efficacité contraceptive et la sécurité du médicament NuvaRing ®. Lorsqu'il est associé à des suppositoires et à des médicaments antifongiques, le risque de rupture de l'anneau augmente légèrement.
Les contraceptifs hormonaux peuvent interférer avec le métabolisme d'autres médicaments. En conséquence, leurs concentrations dans le plasma et les tissus peuvent augmenter (par exemple, la cyclosporine) ou diminuer (par exemple, lamotrigine).
Pour exclure d'éventuelles interactions, vous devez lire les instructions d'utilisation d'autres médicaments.
Recherche en laboratoire
L'utilisation de médicaments hormonaux contraceptifs peut affecter les résultats de certains tests de laboratoire, notamment les indicateurs biochimiques de la fonction hépatique, thyroïdienne, surrénale et rénale ; sur la concentration plasmatique des protéines de transport, par exemple la globuline liant les corticostéroïdes (CBG) et la SHBG ; pour les fractions lipidiques/lipoprotéiques ; sur les indicateurs du métabolisme des glucides ; ainsi que sur les indicateurs de coagulation sanguine et de fibrinolyse. En règle générale, les indicateurs varient dans les limites des valeurs normales.
Utilisation combinée avec des tampons
Les données pharmacocinétiques montrent que l'utilisation de tampons n'affecte pas l'absorption des hormones libérées par l'anneau vaginal NovaRing ®. Dans de rares cas, l'anneau peut être accidentellement retiré lors du retrait du tampon (voir la sous-section « Que faire si l'anneau a été temporairement retiré du vagin » dans la section « Posologie et mode d'administration »).
instructions spéciales
Si l'une des maladies, affections ou facteurs de risque énumérés ci-dessous est présente, les avantages de l'utilisation du médicament NuvaRing ® et les risques possibles pour chaque femme doivent être évalués avant qu'elle ne commence à utiliser le médicament NuvaRing ® . En cas d'exacerbation de maladies, de détérioration de l'état ou de première apparition de l'une des affections énumérées ci-dessous, une femme doit consulter un médecin pour décider de la possibilité d'une utilisation ultérieure du médicament NuvaRing ®.
Troubles circulatoires
L'utilisation de contraceptifs hormonaux peut être associée au développement de thromboses veineuses (thrombose veineuse profonde et embolie pulmonaire) et de thromboses artérielles, ainsi que de complications associées, parfois mortelles.
L'utilisation de n'importe quel COC augmente le risque de développer une thromboembolie veineuse (TEV) par rapport au risque de TEV chez les patients n'utilisant pas de COC. Le plus grand risque de développer une TEV est observé au cours de la première année d'utilisation des COC. Les données d'une vaste étude de cohorte prospective sur l'innocuité de divers COC suggèrent que la plus grande augmentation du risque, par rapport au risque chez les femmes n'utilisant pas de COC, est observée au cours des 6 premiers mois après le début de l'utilisation des COC ou la reprise de leur utilisation après une interruption ( 4 semaines ou plus). Chez les femmes non enceintes n'utilisant pas de contraceptifs oraux, le risque de développer une TEV est de 1 à 5 pour 10 000 femmes-années (WY). Chez les femmes utilisant des contraceptifs oraux, le risque de développer une TEV varie de 3 à 9 cas pour 10 000 femmes. L'augmentation du risque se produit dans une moindre mesure que pendant la grossesse, où le risque est de 5 à 20 pour 10 000 YL (les données sur la grossesse sont basées sur la durée réelle de la grossesse dans des études standard ; sur la base de l'hypothèse que la grossesse dure 9 mois, le risque est de 7 à 27 cas pour 10 000 YL). Chez les femmes en post-partum, le risque de développer une TEV varie de 40 à 65 cas pour 10 000 femmes. La TEV est mortelle dans 1 à 2 % des cas.
Selon les résultats de la recherche, le risque accru de développer une TEV chez les femmes utilisant le médicament NuvaRing ® est similaire à celui chez les femmes utilisant des COC (pour le rapport de risque ajusté, voir le tableau ci-dessous). Une vaste étude observationnelle prospective, TASC (Transatlantic Active Study of the Cardiovascular Safety of NuvaRing ®), a évalué le risque de TEV chez les femmes qui ont commencé à utiliser NuvaRing ® ou des COC, sont passées à NuvaRing ® ou à des COC à partir d'autres contraceptifs, ou ont recommencé à utiliser NuvaRing ® ou COCs utilisation du médicament NuvaRing ® ou COCs dans une population d'utilisateurs typiques. Les femmes ont été suivies pendant 24 à 48 mois. Les résultats ont montré un niveau de risque similaire de développer une TEV chez les femmes utilisant le médicament NuvaRing ® (incidence de 8,3 cas pour 10 000 YL) et chez les femmes utilisant des COC (incidence de 9,2 cas pour 10 000 YL). Pour les femmes utilisant des COC autres que ceux contenant du désogestrel, du gestodène et de la drospirénone, l'incidence de TEV était de 8,5 cas pour 10 000 femmes.
Une étude de cohorte rétrospective initiée par la FDA (US Food and Drug Administration) a montré que l'incidence de TEV chez les femmes ayant commencé à utiliser le médicament NuvaRing ® était de 11,4 cas pour 10 000 YL, tandis que chez les femmes ayant commencé à utiliser des COC contenant du lévonorgestrel, l'incidence de TEV est de 9,2 cas pour 10 000 femmes.
Évaluation du risque (risque relatif) de développer une TEV chez les femmes utilisant le médicament NuvaRing ® par rapport au risque de développer une TEV chez les femmes utilisant des COC
| Etude épidémiologique, population | Comparateur(s) | Risque relatif (RR) (IC à 95 %) |
| TASC (Dinger, 2012) Les femmes qui ont commencé à utiliser le médicament (y compris à nouveau après une pause) et ont abandonné d'autres moyens de contraception. | Tous les COC disponibles pendant l'étude 1. | OU 2 : 0,8 (0,5-1,5) |
| COC disponibles autres que ceux contenant désogestrel, gestodène, drospirénone. | OU 2 : 0,9 (0,4-2,0) | |
| «Étude initiée par la FDA» (Sydney, 2011) Femmes qui ont commencé à utiliser des contraceptifs hormonaux combinés (CHC) pour la première fois au cours de la période d'étude. | COC disponibles pendant la période d'étude 3 . | OU 4 : 1,09 (0,55-2,16) |
| Lévonorgestrel/0,03 mg d'éthinylestradiol. | OU 4 : 0,96 (0,47-1,95) |
2 Prise en compte de l'âge, de l'IMC, de la durée d'utilisation, des antécédents de TEV.
3 Y compris les COC à faible dose contenant les progestatifs suivants : norgestimate, noréthindrone ou lévonorgestrel.
4 En tenant compte de l'âge, du lieu et de l'année d'inclusion dans l'étude.
Il existe des cas extrêmement rares de thrombose d'autres vaisseaux sanguins (par exemple, artères et veines du foie, vaisseaux mésentériques, reins, cerveau et rétine) lors de l'utilisation de COC. On ne sait pas si ces cas sont liés à l'utilisation de COC.
Les symptômes possibles de thrombose veineuse ou artérielle peuvent être un gonflement unilatéral et/ou une douleur dans le membre inférieur, une augmentation locale de la température dans le membre inférieur, une hyperémie ou une décoloration de la peau au membre inférieur ; douleur thoracique soudaine et intense, pouvant irradier vers le bras gauche ; crise d'essoufflement, toux; tout mal de tête inhabituel, sévère et prolongé ; perte soudaine de vision partielle ou totale ; vision double; troubles d'élocution ou aphasie ; vertiges; collapsus, accompagné ou non d'une crise d'épilepsie focale ; faiblesse soudaine ou engourdissement grave d’un côté du corps ou de n’importe quelle partie du corps ; troubles du mouvement; estomac « aigu ».
Facteurs de risque de développement d'une thrombose veineuse et d'une embolie :
- âge;
- présence de maladies dans les antécédents familiaux (thrombose veineuse et embolie chez les frères/sœurs à tout âge ou chez les parents en bas âge). Si une prédisposition héréditaire est suspectée, avant de commencer tout contraceptif hormonal, la femme doit être orientée vers un spécialiste pour consultation ;
- immobilisation prolongée, intervention chirurgicale majeure, toute intervention chirurgicale sur les membres inférieurs ou traumatisme grave. Dans de telles situations, il est recommandé d'arrêter l'utilisation du médicament (en cas d'opération planifiée, au moins 4 semaines à l'avance) avec une reprise ultérieure de l'utilisation au plus tôt 2 semaines après la restauration complète de l'activité motrice ;
- éventuellement thrombophlébite des veines superficielles avec varices.
Il n'existe pas de consensus sur le rôle possible de ces affections dans l'étiologie de la thrombose veineuse.
Facteurs de risque de développement de complications de la thromboembolie artérielle :
- âge;
- le tabagisme (en cas de tabagisme excessif et avec l'âge, le risque augmente encore plus significativement, notamment chez les femmes de plus de 35 ans) ;
- dyslipoprotéinémie;
- obésité (indice de masse corporelle supérieur à 30 kg/m²) ;
- augmentation de la pression artérielle;
- migraine;
- maladie des valvules cardiaques;
- fibrillation auriculaire;
- présence de maladies dans les antécédents familiaux (thrombose artérielle chez les frères/sœurs à tout âge ou chez les parents à un âge relativement précoce). Si une prédisposition héréditaire est suspectée, la femme doit être orientée vers un spécialiste pour consultation avant de commencer tout contraceptif hormonal.
Les facteurs biochimiques pouvant indiquer une prédisposition héréditaire ou acquise à la thrombose veineuse ou artérielle comprennent la résistance activée à la protéine C, l'hyperhomocystéinémie, le déficit en antithrombine III, le déficit en protéine C, le déficit en protéine S, les anticorps antiphospholipides (anticorps anticardiolipine, anticoagulant lupique).
D'autres affections pouvant causer des problèmes circulatoires indésirables comprennent le diabète sucré, le lupus érythémateux disséminé, le syndrome hémolytique et urémique et les maladies inflammatoires chroniques de l'intestin (telles que la maladie de Crohn ou la colite ulcéreuse), ainsi que l'anémie falciforme.
Il est nécessaire de prendre en compte le risque accru de thromboembolie pendant la période post-partum.
Une augmentation de la fréquence ou de la gravité des migraines (qui peuvent être un symptôme prodromique d'accidents vasculaires cérébraux) lors de l'utilisation de contraceptifs hormonaux peut être une raison pour arrêter immédiatement l'utilisation de contraceptifs hormonaux.
Il convient de conseiller aux femmes utilisant des CHC de consulter un médecin si des symptômes possibles de thrombose apparaissent. Si une thrombose est suspectée ou confirmée, l'utilisation de CHC doit être interrompue. Dans ce cas, il est nécessaire d'utiliser une contraception efficace, car les anticoagulants (coumarines) ont un effet tératogène.
Risque de développer des tumeurs
Le facteur de risque le plus important de développer un cancer du col de l’utérus est l’infection par le virus du papillome humain (VPH). Des études épidémiologiques ont montré que l'utilisation à long terme de COC augmente encore ce risque, mais on ne sait pas exactement dans quelle mesure cela est dû à d'autres facteurs, tels que la fréquence accrue des frottis cervicaux et les différences de comportement sexuel, y compris l'utilisation de contraceptifs barrières. On ne sait toujours pas comment cet effet est lié à l'utilisation du médicament NuvaRing ®.
Une méta-analyse de 54 études épidémiologiques a révélé une légère augmentation (1,24) du risque relatif de cancer du sein chez les femmes prenant des contraceptifs oraux hormonaux combinés. Le risque diminue progressivement sur 10 ans après l’arrêt du traitement. Le cancer du sein se développe rarement chez les femmes de moins de 40 ans, de sorte que l'incidence supplémentaire de cancer du sein chez les femmes qui prennent ou ont pris des COC est faible par rapport au risque global de développer un cancer du sein. Le cancer du sein diagnostiqué chez les femmes qui utilisent des COC est cliniquement moins grave que le cancer diagnostiqué chez les femmes qui n'ont jamais utilisé de COC. Le risque accru de cancer du sein peut être dû au diagnostic plus précoce du cancer du sein chez les femmes prenant des COC, aux effets biologiques des COC, ou à une combinaison des deux.
Dans de rares cas, des cas de développement de tumeurs hépatiques bénignes, et encore plus rarement malignes, ont été observés chez des femmes prenant des COC. Dans certains cas, ces tumeurs ont entraîné l’apparition d’hémorragies potentiellement mortelles dans la cavité abdominale. Le médecin doit envisager la possibilité d'une tumeur du foie dans le diagnostic différentiel des maladies chez une femme prenant NuvaRing ® si les symptômes comprennent une douleur aiguë dans la partie supérieure de l'abdomen, une hypertrophie du foie ou des signes de saignement intra-abdominal.
Autres états
- Les femmes souffrant d'hypertriglycéridémie ou d'antécédents familiaux correspondants courent un risque accru de développer une pancréatite lorsqu'elles prennent des contraceptifs hormonaux.
- De nombreuses femmes prenant des contraceptifs hormonaux présentent une légère augmentation de leur tension artérielle, mais les augmentations cliniquement significatives de la pression artérielle sont rares. Un lien direct entre l'utilisation de contraceptifs hormonaux et le développement de l'hypertension artérielle n'a pas été établi. Si, lors de l'utilisation du médicament NuvaRing ®, vous constatez une augmentation constante de la pression artérielle, vous devez contacter votre médecin pour décider s'il est nécessaire de retirer l'anneau vaginal et de prescrire un traitement antihypertenseur. Avec un contrôle adéquat de la pression artérielle à l'aide d'antihypertenseurs, il est possible de reprendre l'utilisation du médicament NuvaRing ®.
- Au cours de la grossesse et lors de l'utilisation de contraceptifs oraux combinés, l'apparition ou l'aggravation des affections suivantes a été constatée, bien que leur relation avec l'utilisation de contraceptifs n'ait pas été définitivement établie : jaunisse et/ou démangeaisons provoquées par une cholestase, formation de calculs biliaires, porphyrie. , lupus érythémateux disséminé, syndrome hémolytique et urémique, chorée de Sydenham (chorée mineure), herpès gravidique, perte auditive due à l'otospongiose, angio-œdème (héréditaire).
- Les maladies hépatiques aiguës ou chroniques peuvent servir de raison pour arrêter le médicament NuvaRing ® jusqu'à ce que les indicateurs de la fonction hépatique se normalisent. La récidive de l'ictère cholestatique, précédemment observée au cours de la grossesse ou lors de l'utilisation d'hormones sexuelles, nécessite l'arrêt du médicament NuvaRing ® .
- Bien que les œstrogènes et les progestatifs puissent influencer la résistance périphérique à l’insuline et la tolérance tissulaire au glucose, il n’existe aucune preuve étayant la nécessité de modifier le traitement hypoglycémiant pendant l’utilisation de contraceptifs hormonaux. Cependant, les femmes diabétiques doivent être sous surveillance médicale constante lorsqu'elles utilisent le médicament NuvaRing ® , en particulier au cours des premiers mois de contraception.
- Il existe des preuves d'une aggravation de la maladie de Crohn et de la colite ulcéreuse avec l'utilisation de contraceptifs hormonaux.
- Dans de rares cas, une pigmentation de la peau du visage (chloasma) peut survenir, surtout si elle est survenue plus tôt au cours de la grossesse. Les femmes prédisposées au développement du chloasma doivent éviter de s'exposer au soleil et aux rayons ultraviolets lorsqu'elles utilisent NuvaRing ®.
- Les conditions suivantes peuvent empêcher l'insertion correcte de l'anneau ou provoquer sa chute : prolapsus cervical, hernie vésicale et/ou rectale, constipation chronique sévère.
- Dans de très rares cas, des femmes ont involontairement inséré l'anneau vaginal NuvaRing ® dans l'urètre et éventuellement dans la vessie. Lorsque des symptômes de cystite apparaissent, il est nécessaire d’envisager la possibilité d’une mauvaise insertion de l’anneau.
- Des cas de vaginites ont été décrits lors de l'utilisation du médicament NuvaRing®. Il n'existe aucune preuve que le traitement de la vaginite affecte l'efficacité de l'utilisation du médicament NuvaRing ® , ni aucune preuve de l'influence de l'utilisation du médicament NuvaRing ® sur l'efficacité du traitement de la vaginite.
- De très rares cas de retrait difficile de l’anneau ont été décrits et ont nécessité son retrait par un professionnel de la santé.
Examen/consultation médicale
Avant de prescrire le médicament NuvaRing ® ou de reprendre son utilisation, vous devez examiner attentivement les antécédents médicaux de la femme (y compris les antécédents familiaux) et procéder à un examen gynécologique pour exclure une grossesse. Il est nécessaire de mesurer la tension artérielle, de procéder à un examen des glandes mammaires et des organes pelviens, y compris un examen cytologique des frottis cervicaux et certains tests de laboratoire, pour exclure les contre-indications et réduire le risque d'effets secondaires possibles du médicament. La fréquence et la nature des examens médicaux dépendent des caractéristiques individuelles de chaque patient, mais les examens médicaux sont effectués au moins une fois tous les 6 mois. Une femme doit lire le mode d'emploi et suivre toutes les recommandations. La femme doit être informée que NuvaRing ® ne protège pas contre l'infection par le VIH (SIDA) et d'autres maladies sexuellement transmissibles.
Efficacité réduite
L'efficacité du médicament NuvaRing ® peut diminuer si le régime n'est pas suivi ou si un traitement concomitant est effectué.
Contrôle de cycle réduit
Pendant l'utilisation du médicament NuvaRing ®, des saignements acycliques (spottings ou saignements soudains) peuvent survenir. Si un tel saignement est observé après des cycles réguliers lors de l'utilisation correcte du médicament NuvaRing ®, vous devez contacter votre gynécologue pour mener les études diagnostiques nécessaires, notamment pour exclure une pathologie organique ou une grossesse. Un curetage diagnostique peut être nécessaire.
Certaines femmes ne saignent pas après le retrait de l'anneau. Si le médicament NuvaRing ® a été utilisé conformément aux instructions, il est peu probable que la femme soit enceinte. Si les recommandations des instructions ne sont pas respectées et qu'il n'y a pas de saignement après le retrait de l'anneau, ainsi que s'il n'y a pas de saignement pendant deux cycles consécutifs, une grossesse doit être exclue.
Effets de l'éthinylestradiol et de l'étonogestrel sur un partenaire sexuel
Les effets pharmacologiques possibles et l'étendue de l'exposition à l'éthinylestradiol et à l'étonogestrel chez les partenaires sexuels masculins (en raison de l'absorption par le tissu pénien) n'ont pas été étudiés.
Dommages à l'anneau
Dans de rares cas, lors de l'utilisation du médicament NuvaRing ®, une rupture d'anneau a été observée. Le noyau du médicament NuvaRing ® est solide, son contenu reste donc intact et la libération d'hormones ne change pas de manière significative. Si l'anneau se rompt, il tombe généralement hors du vagin (voir les recommandations de la sous-section « Que faire si l'anneau a été temporairement retiré du vagin » dans la section « Posologie et mode d'administration »). Si l'anneau se rompt, un nouvel anneau doit être inséré.
L'anneau tombe
Parfois, l'anneau vaginal NuvaRing ® peut tomber du vagin, par exemple s'il est mal inséré, lorsqu'un tampon est retiré, pendant un rapport sexuel ou en raison d'une constipation sévère ou chronique. A cet égard, il est conseillé à une femme de vérifier régulièrement la présence de l'anneau vaginal NuvaRing ® dans le vagin. Si l'anneau vaginal NuvaRing ® tombe du vagin, vous devez suivre les recommandations de la sous-section « Que faire si l'anneau a été temporairement retiré du vagin » dans la rubrique « Mode d'administration et posologie ».
Impact sur la capacité de conduire des véhicules et d’utiliser des machines
Sur la base des informations sur les propriétés pharmacodynamiques du médicament NuvaRing ®, on peut s'attendre à ce qu'il n'affecte pas l'aptitude à conduire des véhicules et à utiliser des machines.
Formulaire de décharge
Anneaux vaginaux 0,015 mg + 0,120 mg/jour. 1 anneau est emballé dans un sachet en aluminium imperméable, recouvert à l'intérieur d'une couche de polyéthylène basse densité et à l'extérieur d'une couche de polyéthylène téréphtalate (PET). 1 ou 3 sachets par boîte en carton avec mode d'emploi.
Conditions de stockage
Conserver à une température de 2 à 8 °C.
Garder hors de la portée des enfants.
Date de péremption
3 années.
Ne pas utiliser après la date de péremption indiquée sur l'emballage.
Conditions de vacances
Sur ordonnance.
Personne morale au nom de laquelle le certificat d'immatriculation a été délivré
N.V. Organon, Pays-Bas
Fabricant
Produit :
N.V. Organon, Pays-Bas
Contrôle qualité des versions :
N.V. Organon, Pays-Bas
N.V. Organon, Kloosterstraat 6, 5349 AB, Oss, Pays-Bas
ou
Organon (Ireland) Ltd., Irlande
Organon (Irlande) Ltd., P.O. Boîte postale 2857, Drynam Road, Swords, Co. Dublin, Irlande
Les plaintes des consommateurs doivent être envoyées à :
MSD Pharmaceutique LLC
St. Pavlovskaya, 7, bâtiment 1
Moscou, Russie, 115093
Ou des questions fréquemment posées sur l'anneau hormonal NuvaRing, que le médecin entend à chaque rendez-vous.
Qu’est-ce que NuvaRing ?
est un anneau élastique qui s’insère profondément dans le vagin. Le système est installé dès les premiers jours du cycle menstruel et reste dans le tractus génital pendant 21 jours. L'anneau contraceptif contient les hormones sexuelles féminines œstrogène et progestérone. Ces substances sont progressivement libérées et pénètrent dans la circulation sanguine, bloquant l’ovulation et rendant une grossesse impossible. Les hormones rendent également la glaire cervicale visqueuse, de sorte que les spermatozoïdes agiles ne pénètrent pas à l'intérieur et ne remplissent pas leur fonction.
Aujourd'hui, l'anneau vaginal NuvaRing est considéré comme l'un des contraceptifs les plus efficaces avec une quantité minimale d'hormones. Ce fait rend le système populaire auprès des femmes jeunes et plus âgées. Que devez-vous savoir sur NuvaRing et comment utiliser correctement ce contraceptif ?
À qui convient NuvaRing ?
L’anneau contraceptif est un bon choix pour différentes catégories de femmes :
- Femmes jeunes et nullipares avec un seul partenaire sexuel.
- Après l'accouchement et la fin de l'allaitement.
- En période préménopausique (en l'absence de pathologie chronique pouvant devenir une contre-indication).
Pourquoi NuvaRing est-il meilleur que les pilules contraceptives ?
L'anneau vaginal présente trois avantages évidents par rapport aux COC de composition similaire :
- Le dosage d’oestrogène est inférieur à celui de n’importe quelle pilule hormonale.
- Le médicament ne traverse pas le tractus gastro-intestinal et n'affecte pas la digestion.
- Vous n’avez pas besoin de vous rappeler de prendre les pilules tous les jours : insérez simplement l’anneau une fois et oubliez-le pendant 21 jours.
NuvaRing peut-il être administré aux mères qui allaitent ?
Les instructions d'utilisation de l'anneau contraceptif ne recommandent pas l'utilisation de NuvaRing pendant l'allaitement. Vous devez attendre la fin de l'allaitement et insérer ensuite l'anneau. Les mères qui allaitent peuvent utiliser des mini-pilules (préparations purement progestatives) comme contraception. N'oubliez pas les préservatifs.
Une femme peut-elle mettre elle-même un anneau contraceptif ou doit-elle consulter un médecin ?
NuvaRing est simple, pratique et abordable. N’importe quelle femme peut insérer elle-même une bague sans aucun problème. Pour ce faire, vous devez prendre une position confortable - accroupi, debout ou allongé - et insérer l'anneau le plus profondément possible. En cas de difficultés, vous pouvez prendre rendez-vous avec un médecin. Le médecin insérera l'anneau et expliquera ensuite en détail au patient comment le faire à la maison.
Un homme peut-il sentir la bague pendant les rapports sexuels ?
Non, NuvaRing n’est pas du tout ressenti pendant les rapports sexuels.
Une femme peut-elle sentir l’anneau vaginal ?
Non, si le NuvaRing est correctement installé, il n’est pas ressenti dans le vagin.
Pourquoi la bague ne tombe-t-elle pas ?
NuvaRing, inséré profondément, est solidement fixé dans le vagin par les muscles. De plus, l'anneau se trouve horizontalement dans le tractus génital, comme sur une étagère, et le risque qu'il tombe est extrêmement faible.
L'anneau peut-il tomber ?
C'est rare, mais ça arrive. Dans ce cas, vous devez laver l'anneau avec de l'eau tiède ou froide et le réinsérer soigneusement dans le vagin. L'effet contraceptif ne souffre pas si moins de 3 heures se sont écoulées depuis la chute de l'anneau.
L’anneau est tombé, mais je n’ai pas eu le temps de le remettre rapidement en place. Ce qu'il faut faire?
Si plus de 3 heures se sont écoulées depuis que l'anneau est tombé ou a été retiré, vous devez procéder selon le schéma suivant :
- Si un tel problème survient au cours de la 1ère ou de la 2ème semaine d'utilisation de l'anneau NuvaRing, vous devez le remettre à sa place le plus rapidement possible. L'effet contraceptif du médicament est réduit et pendant un certain temps, la femme ne sera plus protégée contre une grossesse non désirée. Il est recommandé d'utiliser en plus un préservatif pendant les 7 prochains jours.
- Si l'anneau tombe au cours de la 3ème semaine d'utilisation, il doit être jeté et un nouveau doit être immédiatement inséré. Dans ce cas, il n’y aura pas de saignements de type menstruel, mais de rares saignements peuvent être observés. C’est normal, il n’y a pas lieu de paniquer. L'anneau est retiré après les 21 jours prescrits, puis une pause de 7 jours est prise et un nouveau médicament est introduit.
- Si une femme ne souhaite pas recevoir un nouvel anneau immédiatement, elle peut attendre les saignements de privation et insérer NuvaRing après 7 jours. Cette option n'est possible que si l'anneau ne tombe jamais pendant les deux premières semaines. Si le problème est déjà survenu, voir le point 2.
Est-il possible de retirer un anneau vaginal pendant un rapport sexuel ?
Oui, mais cela n’a aucun sens, car NuvaRing ne se sent ni comme une femme ni comme un homme. Si la bague est néanmoins retirée, elle doit être restituée dans les 2-3 heures et au plus tard.
Un NuvaRing peut-il s’enfoncer trop profondément ?
Non, l’anneau contraceptif est solidement fixé au vagin. Il ne tombera pas dans l'utérus, puisque l'entrée de l'organe reproducteur est bloquée par un pharynx fermé. L'anneau n'a nulle part où sortir du tractus génital de la femme et même pendant les rapports sexuels, il ne pénétrera pas trop profondément.
Est-il possible de laisser l’anneau NuvaRing dans le vagin pendant 4 semaines ?
Ceci est acceptable car l'effet contraceptif du système dure jusqu'à 28 jours. Au bout de 4 semaines, l'anneau doit être retiré : les niveaux d'hormones chutent et la femme perd sa protection contre une grossesse non désirée.
Est-il possible de congeler un NuvaRing ?
Vous pouvez conserver l’anneau contraceptif au réfrigérateur jusqu’à 12 heures. Il n'est pas recommandé de congeler le système au congélateur. Si vous devez emporter un contraceptif avec vous (par exemple, lorsque vous voyagez dans une autre ville), utilisez un sac isotherme spécial.
Est-il possible d'annuler des périodes ?
Oui, vous pouvez insérer une nouvelle bague sans une semaine de pause. Les menstruations ne viendront pas, mais des spottings peuvent survenir au milieu du cycle. Le nouvel anneau peut être laissé dans le vagin pendant 21 jours (comme d'habitude).
Comment reporter la date des règles lors de l'utilisation de l'anneau NuvaRing ?
C'est très simple : il suffit d'insérer une nouvelle bague non pas après 7 jours, mais par exemple 5 ou 6 après avoir retiré la précédente. Il est important de le savoir : plus la pause est courte, plus la probabilité de spotting en milieu de cycle est élevée.
Les filles de moins de 18 ans peuvent-elles utiliser l’anneau contraceptif ?
La sécurité de NuvaRing n’a pas été étudiée chez les adolescents. Une consultation en personne avec un médecin est requise.
Dois-je utiliser un anneau en cas de prolapsus utérin ?
Avec cette pathologie, le NuvaRing peut tomber. Il est recommandé d'utiliser d'autres moyens de contraception.
Pourquoi ne pouvez-vous pas prendre d'antibiotiques si vous avez un anneau ?
Ce n'est pas tout à fait vrai. Si le médecin a prescrit des médicaments antibactériens, ils doivent être pris. Le problème est que lors de l'utilisation de certains antibiotiques (notamment l'ampicilline et la tétracycline), l'effet contraceptif diminue. Pendant qu'une femme prend des antibiotiques, elle doit également utiliser des préservatifs - pendant toute la durée du traitement et pendant 7 jours après la fin du traitement.
Un NuvaRing peut-il se briser ?
Oui, c'est possible. Le risque de rupture d'anneau augmente avec l'utilisation simultanée de suppositoires vaginaux contre une infection fongique (muguet). Pendant le traitement, vous devez également utiliser des préservatifs et surveiller l'état du NuvaRing.
Puis-je utiliser un anneau contraceptif avec des tampons ?
Oui, l’utilisation de tampons n’affecte pas la fonctionnalité de NuvaRing. Dans de rares cas, l'anneau peut tomber après avoir retiré le tampon.
NuvaRing provoque-t-il le cancer du col de l'utérus ?
On pense que la principale cause des lésions malignes du col de l'utérus est le virus du papillome humain (VPH), mais pas l'utilisation de contraceptifs hormonaux. Les statistiques montrent que les femmes qui ont utilisé NuvaRing sont plus susceptibles de développer un cancer du col de l'utérus, mais les gynécologues attribuent cela à des examens réguliers effectués par un médecin et à des tests annuels (frottis pour l'oncocytologie). Il convient de noter que dans cette situation, la maladie est généralement détectée à un stade précoce, lorsqu'elle est beaucoup plus facile à guérir.
À quelle vitesse pouvez-vous tomber enceinte après avoir retiré le NuvaRing ?
La restauration de la fertilité se produit dans les 1 à 3 mois suivant l'arrêt du médicament. Cela signifie qu'une femme peut tomber enceinte dès le premier cycle après avoir retiré l'anneau. Dans certains cas, la conception d'un enfant survient après 3 à 12 mois.
Comment évolue le cycle menstruel après la pose d’un anneau vaginal ?
Après l’introduction de NuvaRing, la libération progressive des hormones commence. Le cycle menstruel devient monotone. Le niveau de vos propres hormones reste stable. En règle générale, les menstruations deviennent moins abondantes et leur durée diminue. Des saignements de type menstruel dus à NuvaRing surviennent tous les 28 jours strictement selon le calendrier.
Combien coûte NuvaRing ?
Le prix moyen d'un anneau contraceptif est d'environ 1 000 roubles.
